重磅丨EUDAMED注冊模塊將于12月1日開放.EUDAMED 數據庫是由歐盟委員會為配合MDR和IVDR實施而開發的。數據庫包含了6個模塊,其中器械注冊將是第一個開放的模塊。

1 誰需要在EUDAMED進行注冊?
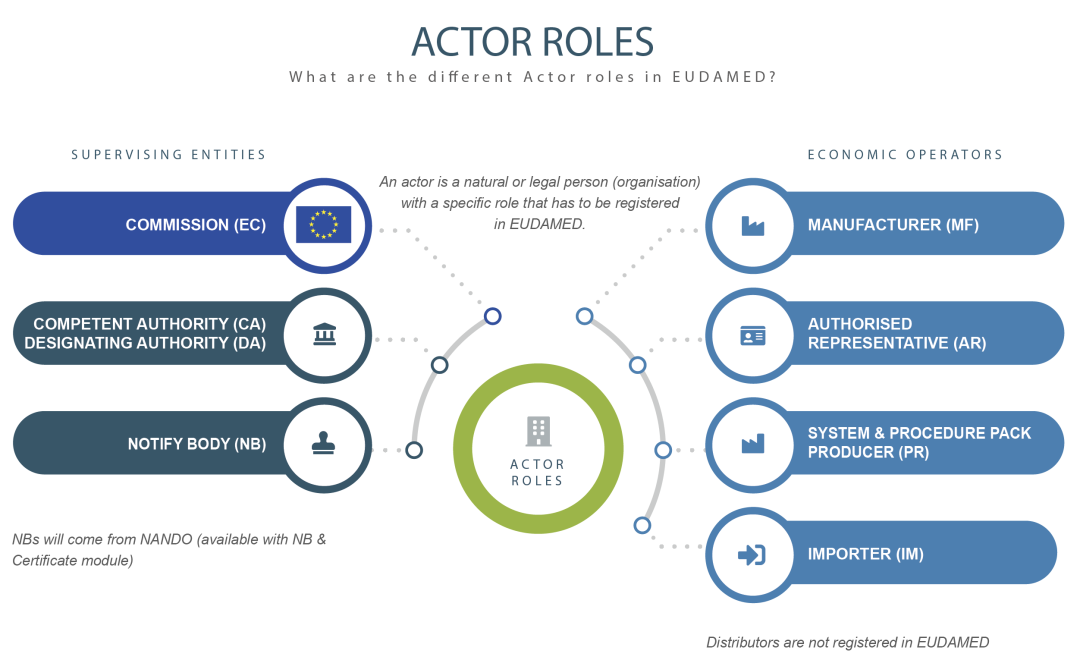
EUDAMED數據庫相關方主要包括監管機構和經濟運營商。其中監管機構包括歐盟委員會、各國的主管當局和公告機構;經濟運營商主要包括:制造商、歐盟授權代表、套裝類產品的組裝生產商以及進口商。這幾類經濟運營商都需要在EUDAMED數據庫系統進行注冊,而經銷商則不需要再EUDAMED數據庫進行注冊。
2 注冊第一步先獲得身份證號
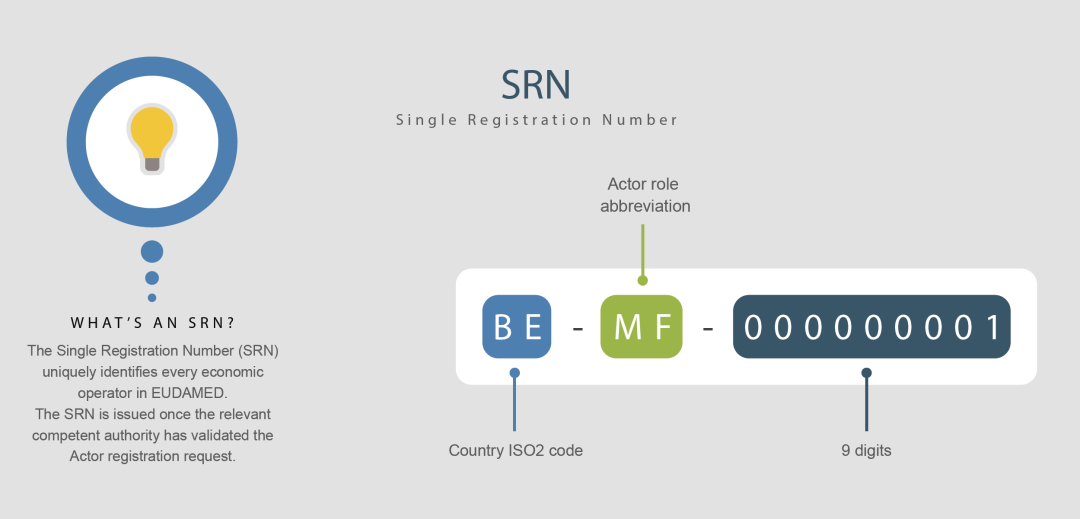
SRN 唯一注冊碼,是在EUDAMED數據庫中對各類經濟運營商進行識別的唯一編碼。SRN代碼的結構如下,為國家代碼+角色代碼+9位數字代碼。
其中角色代碼包括:
制造商---MF
授權代表---AR
套裝類組裝廠---PR
進口商---IM
SRN應有相應的經濟運營商提出申請,經過相應的主管當局確認后分配。
3 一個公司申請一個SRN,對嗎?
需要說明的是,如果同一家公司承擔了幾個不同的經濟運營商的角色,那么他應該分別申請對應的SRN。例如,如果該比利時企業既是制造商,又是進口商,那么申請SRN就有兩個:
BE-MF-000000002(作為制造商)
BE-IM -000000003(作為進口商)
4非歐盟制造商能直接遞交申請嗎?
非歐盟制造商并不能直接提交SRN的申請,而是需要通過歐盟授權代表核實后,由歐盟授權代表來提交申請給成員國主管當局來進行審批。當然,歐盟授權代表需要事先獲得自己的SRN。
轉載注明:http://www.rkdu.cn/








