1.若知悉送檢產品對應的產品國家標準或行業標準,如何搜索?
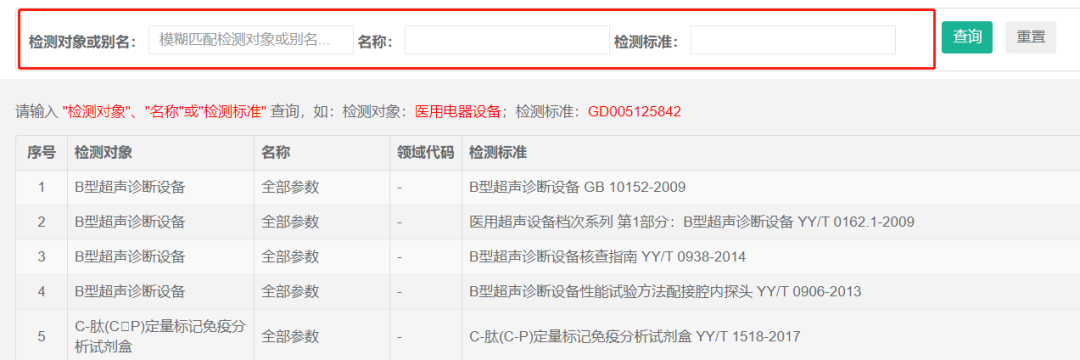
進入器檢院首頁網上大廳承檢目錄查詢界面,在“檢測標準”欄搜索國家標準或行業標準標準號的數字,不要連帶YY或GB一起搜,有可能因為空格等不匹配導致搜索不到。
2.若不知悉送檢產品對應的產品國家標準或行業標準,如何搜索?
進入器檢院首頁網上大廳承檢目錄查詢界面,在“檢測對象或別名”欄搜索產品名稱關鍵字,不要填寫產品全名,有可能因為多一個字或少一個字不匹配導致搜索不到。
3.什么情況下可直接受理?
若產品技術要求中所有檢測項目或引用的標準均在我院承檢范圍內,則說明該產品我院有承檢能力,可受理。
4.什么情況下需經過技術審核才能受理?
若產品技術要求中檢測項目或引用的標準僅部分或均不在我院承檢范圍內,則需等到資料審核階段,受理人員通過審核企業上傳的資料或通過我院技術委員會內部評審方可確認檢測能力,確認是否受理。建議在預約前或排隊中參與器檢院“技術預咨詢開放日”活動(詳見醫療器械檢驗提示之三 技術預咨詢服務流程),提前確認是否可以受理。
5.器檢院的注冊檢驗受理原則是什么?
器檢院的注冊檢驗受理原則是只要有檢測能力的注冊檢驗項目一律受理。
6.什么情況下注冊報告蓋CMA章?
按照《國家藥監局綜合司關于明確醫療器械檢驗工作規范標注資質認定標志有關事項的通知》(藥監綜科外函〔2020〕746號)文件規定,檢驗依據是我院承檢目錄內的國、行標的檢驗報告,加蓋CMA資質章;檢驗依據為產品技術要求,不加蓋CMA章,報告首頁會增加備注:該產品技術要求不涉及/部分涉及國家標準、行業標準,不能直接作為資質認定許可的依據,但本實驗室對報告涉及的檢驗項目具備相應的承檢能力。
標簽:醫療器械檢測
轉載注明:http://www.rkdu.cn/







